無機化学のハロゲンに関する問題で、塩素Cl2の発生法についてよく聞かれます。ここでは、実験の方法もあわせて勉強していきます。
塩素Cl2の実験室的製法
実験室での塩素Cl2のつくり方は次の2つの方法があります。
- さらし粉や高度さらし粉に塩酸を加える。
CaCl(ClO)・H2O+2HCl→CaCl2+2H2O+Cl2
CaCl(ClO)2・2H2O+4HCl→CaCl2+4H2O+2Cl2 - 酸化マンガンに(Ⅳ)に濃塩酸を加えて加熱する。
MnO2+4HCl→MnCl2+2H2O+Cl2
反応式が書けるようにしっかりと練習してください。
さらし粉・高度さらし粉に塩酸
次亜塩素酸ClO–を含んでいるさらし粉や高度さらし粉に塩酸を加えると次のような反応が起きます。
H++ClO–+H++Cl- ⇄ Cl2+H2O
さらし粉や高度さらし粉で塩酸を発生させる際に加熱は必要でありません。
酸化マンガン(Ⅳ)に濃塩酸を加える。
酸化マンガン(Ⅳ)に濃塩酸を加えると、酸化還元反応が起こり塩素が発生します。
- 2Cl– → Cl2+2e–
- MnO2+4H++2e– → Mn2++2H2O
半反応式どうしを足し合わせ、イオン反応式をつくり、残りのイオンを足してあげれば化学反応式が完成します。酸化マンガン(Ⅳ)と濃塩酸で塩素を発生させる場合、加熱が必要になります。
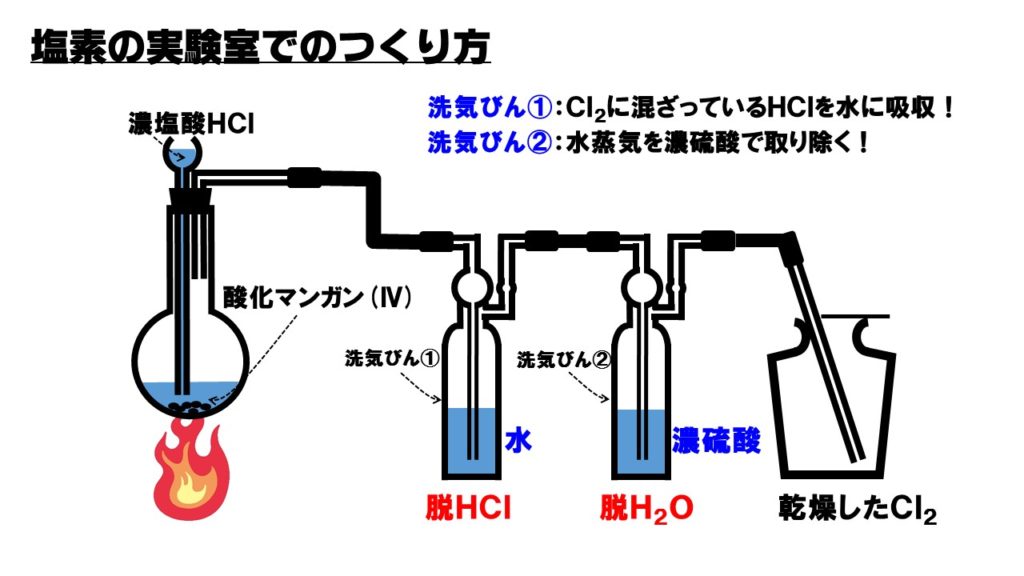
塩素の発生装置
発生した気体を水に通し塩化水素HClを除去した後、濃硫酸に通して水H2Oを除去することで、塩素を精製することができ、乾いた塩素を得ることができます。
塩素の発生法の練習問題
- さらし粉と塩酸で塩素を発生させるときの化学反応式をかけ。
- さらし粉で塩素を発生させる場合、加熱は必要か。
- 酸化マンガン(Ⅳ)と濃塩酸で塩素を発生させるときの化学反応式をかけ。
- 3で出てきた気体は、最初水に通すか、濃硫酸に通すか。
- 出てきた気体を水に通す理由を答えよ。
- 出てきた気体を濃硫酸に通す理由を答えよ。
- 塩素の捕集法で一番適するものは何か。
解答
- CaCl(ClO)・H2O+2HCl→CaCl2+2H2O+Cl2
- 必要ではない
- MnO2+4HCl→MnCl2+2H2O+Cl2
- 水に通す
- 塩化水素を除去するため
- 水蒸気を除去するため
- 下方置換法


コメント