大学受験や模試、定期試験で出題されやすい内容を丁寧に解説していきます。今日は「酵素」でも定番の問題である「反応速度」のグラフに関する問題です。では、早速見ていきましょう。
酵素と反応速度
酵素と反応速度に関する問題では、生成物量や反応速度などに関するグラフが出題されます。基質の量を増やした場合や、酵素の量を増やした場合など、さまざまに条件を変えて、グラフがどのように変化するのかを問われます。
基本用語の復習
反応速度や生成物量のグラフに関する問題に入る前に、まずは簡単な基礎知識の整理を行いましょう。用語の意味や基礎的な内容が定着していないと混乱を招きます。
酵素
生体内でつくられ触媒のことで、物質の反応を手助けしてくれる物質、言い換えると活性化エネルギーを下げてくれる物質になります。触媒ですので、自らは変化せず消費されたりはしません。
最適温度
酵素は主にタンパク質でつくられています。お肉や卵などと同じですので、熱に弱く、高温で変性し(熱変性)はたらきを失います(失活)。酵素が最もよく働く温度を「最適温度」といい35℃~40℃付近になります。
最適pH
タンパク質は、酸やアルカリによっても変性します。お刺身にレモンのスライスが乗っていると、そこだけ白く変色するのはそのためです。したがって酵素にも最も働きやすいpHがあり、それを最適pHといいます。主な酵素の最適pHは次の通りです。
- 唾液アミラーゼ…pH7
- ペプシン…pH2
- トリプシン…pH8
- 植物のアミラーゼ…pH6
基質
酵素がはたらきかける物質のことです。例えば、胃液に含まれる消化酵素であるペプシンの場合、基質はタンパク質になります。
生成物
酵素のはたらきで基質が変化して生じた物質のことを生成物といいます。タンパク質(基質)がペプシン(酵素)のはたらきでペプトン(生成物)になります。
基質特異性
酵素がはたらく基質が決まっていることを基質特異性といいます。酵素と基質の結合部位である活性部位(活性中心)の形が決まっていて、この活性部位に結合できる基質のみが酵素のはたらきを受けることになります。
酵素-基質複合体
酵素と基質が活性部位で結合している状態のものを、酵素-基質複合体といいます。酵素は、酵素-基質複合体をつくり基質を分解し生成物をつくりだします。
反応速度
酵素が一定時間にどのくらいの基質を生成物に変化させるかを示したものです。酵素の量が一定の場合、すべての酵素が酵素-基質複合体をつくると、反応速度は一定になります。
競争的阻害(拮抗的阻害)
酵素の活性部位を基質と阻害物質が取りあう場合、基質が結合できなくなり反応が阻害される現象です。
非競争的阻害(非拮抗的阻害)
アロステリック部位など、阻害物質が酵素の活性部位以外に結合し、酵素反応を阻害する現象です。
以上が、ここでの基本的な用語です。まだまだ多くの用語がありますが、最低限これだけマスターしていれば、グラフの問題は理解できます。
時間と生成物量のグラフ
縦軸に生成物量を、横軸に時間変化を取ったグラフです。時間とともに基質が分解され、生成物が増加していきます。基質が分解されつくしてしまうと、それ以降は生成物が増えなくなるのが特徴です。
この状態になれば、酵素を追加しても基質がもうありませんので生成物量は増加しませんが、基質を追加してあげると生成物量は増加します。
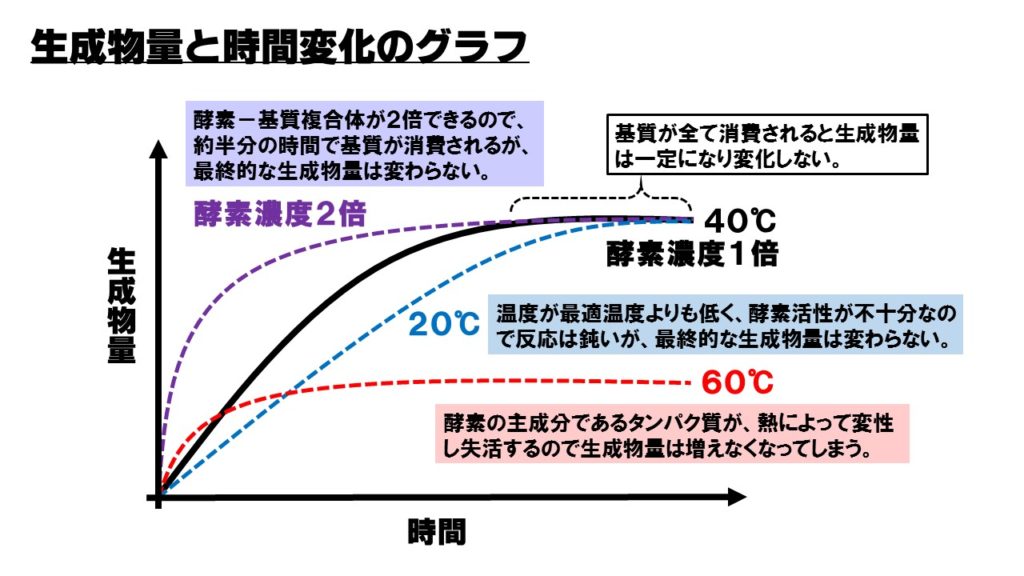
最終的な生成物量
基質が酵素によって分解されて、最終的な生成物になりますが、最終的な生成物量は、生成物のもととなる基質の量が変わらない場合一定で変わりません。基質が分解されつくせばそれ以上生成物が増えないのはわかりますよね。
- 基質を半分→生成物量も半分
- 基質を2倍→生成物量も2倍
- 酵素を2倍→生成物量は変わらない
温度を変えると
温度を変えると、酵素の活性度合いが変わりますので、基質の分解スピードに差が出てきます。高温になればなるほど、基質の分解スピードは速くなりますが、最終的な生成物量は変わりません。したがってグラフの傾きだけが変化する形になります。
また、酵素の主成分はタンパク質ですので、60℃以上にすると酵素が熱によって変性し失活します。そうなれば基質を分解できなくなりますので、生成物量は少なくなってしまいます。
- 温度を20℃にする→グラフの傾きが緩やかになるが生成物量は変わらない
- 温度を60℃にする→グラフの傾きは急になるが、やがて失活し生成物ができなくなる
pHを変えても温度と同じような変化がグラフに見られるようになります。
酵素の濃度を変えると
酵素の濃度を変えても、最終的な生成物量は変化しません。しかし、酵素の量が増えると、一度にできる酵素-基質複合体の数が増加するので、一度にたくさんの生成物をつくりだすことができます。したがって、酵素の濃度を2倍にすると、約半分の時間ですべての基質が分解できます。
- 酵素濃度2倍→すべての基質が分解されるまでの時間が半分になる
- 酵素濃度半分→すべての基質が分解されるまでの時間が2倍になる
反応速度のグラフ
反応速度とは、一定時間あたりに生成物がどれくらいできるかを表したものです。反応速度は酵素-基質複合体の量で決まります。酵素-基質複合体がたくさんできれば、それだけ単位時間あたりに分解できる基質の量が増え、単位時間当たりの生成物量も増加します。
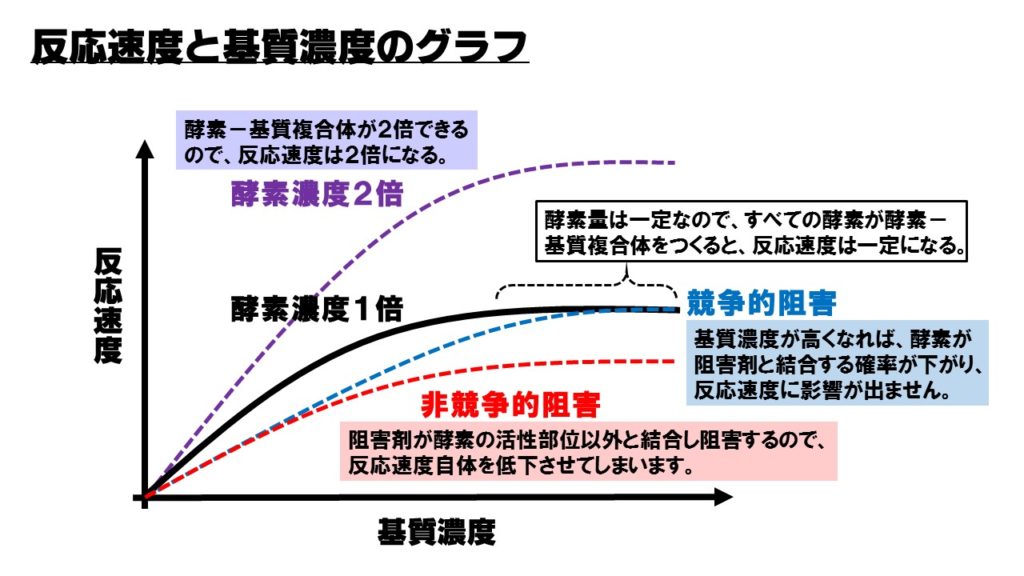
基質濃度がある一定量を超えると、反応速度が一定になるのは、すべての酵素が酵素-基質複合体を形成するためです。
酵素濃度を変えると
酵素濃度を変化させると、できる酵素-基質複合体の数が変化しますので反応速度が変わります。
- 酵素濃度2倍→反応速度2倍
- 酵素濃度半分→反応速度半分
阻害剤を入れると
阻害剤が、酵素の活性部位と結合する競争的阻害か、酵素の活性部位以外のアロステリック部位などに結合する非競争的阻害かでグラフの特徴が変わってきます。
競争的阻害の場合、基質濃度が低いときは、酵素と阻害剤が出会う確率が高いので、酵素は阻害剤のはたらきをもろに受けてしまいます。しかし、基質濃度が高くなると、酵素と基質ばかりが出会うようになり、阻害剤が酵素と結合しにくくなります。そのため、基質濃度が十分に大きい場合は、阻害剤の影響が出にくく、反応速度は阻害剤がない場合と変わらなくなります。
非競争的阻害の場合、基質が結合しない部位と阻害剤が結合するので、基質濃度に関係なく酵素のはたらきを阻害します。したがって反応速度は基質濃度が十分に多い場合でも、反応速度は低下します。
- 競争的阻害あり→反応速度は基質が少ない場合は低下、基質が多い場合は影響がない
- 非競争的阻害あり→反応速度が低下、基質が多い場合も反応速度が低下する

コメント