化学の固体の学習内容である、結晶について見ていきましょう。今回は金属結晶です。3つの単位格子である体心立方格子・面心立方格子・六方細密構造の基本をまずはおさえましょう。
金属結晶の単位格子
金属結合をしている物質は、自由電子がすべての金属原子によって共有されてできた金属結晶つくっています。この結晶をつくっている金属原子がどのように並んでいるかを示したものが結晶格子と呼ばれるものです。
結晶格子は、結晶構造の最小単位である単位格子が繰り返されてできており、単位格子は次の3種類を覚えましょう。
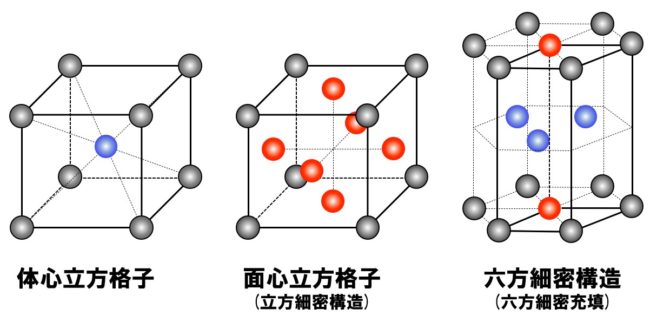
- 体心立方格子は、立方体の8つの頂点と、立方体の中心に金属原子が配置されています。
- 面心立方格子は、立方体の8つの頂点と、立方体をつくる4つの面の中心に金属原子が配置されています。また、面心立方格子は見方を変えると、立方細密構造とも呼ばれます。ここは次回以降詳しく説明します。
- 六方細密構造は、正六角柱の12の頂点と、底面である2つの正六角形の面の中心、正六角柱の中に3つ金属原子が配置されています。六方細密構造の単位格子は上図の実線部分で、正六角柱の3分の1である四角柱になります。
具体的に、どの金属原子がどの単位格子になるのかは次の通りです。
- 体心立方格子…アルカリ金属、Fe(常温)
- 面心立方格子…Al、Fe(高温)、Cu、Ag、Au
- 六方細密構造(六方細密充填)…Mg、Zn
単位格子の原子数
単位格子の中にある原子数は、体心立方格子では2個、面心立方格子では4個、六方細密構造では2個になります。
●体心立方格子の単位格子内の原子数
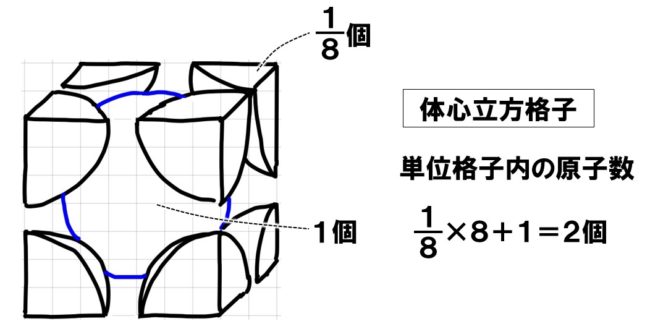
8つの頂点には、8分の1の原子が配置されているので合計1個、立方体の中心に1個の原子がすっぽり入っているので、単位格子内には合計2個の原子が入っていることになります。
●面心立方格子の単位格子内の原子数
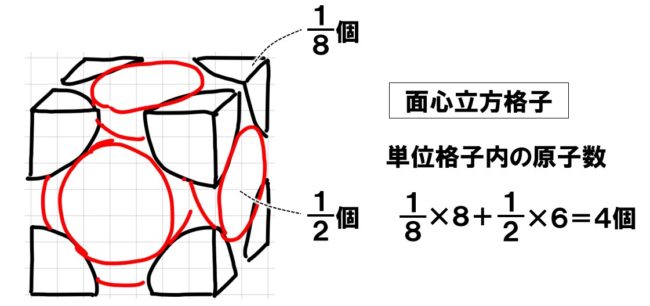
8つの頂点には、8分の1の原子が配置されているので合計1個、立方体の6つの側面に、2分の1の原子がそれぞれ配置されているので合計3個、したがって、面心立方格子の単位格子内には、合計4個の原子が入っていることになります。
●六方細密構造の単位格子内の原子数
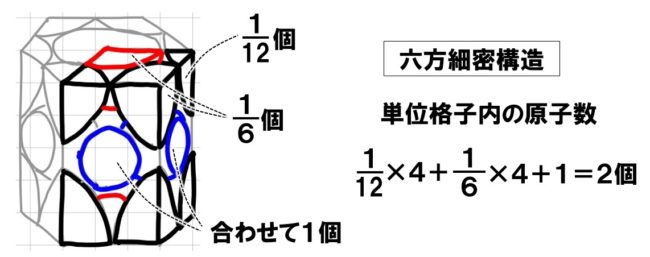
六方細密構造の単位格子は、上図のような正六角柱の3分の1にあたります。この単位格子内には、頂点にある中心角60°の12分の1個の原子が4個、中心角120°の6分の1個の原子が4個、また、六角柱内にある3つの原子は、その3分の1が単位格子内に含まれるので1個、合計2個の原子が六方細密構造の単位格子内に含まれています。
単位格子ではありませんが、六方細密構造の正六角柱の中には2個×3=6個、原子が入っていることになりますね。
単位格子の配位数
配位数とは、1個の原子が最近接している原子の数のことです。簡単にいうと、1つの原子をとり囲む原子の数のことです。配位数は、体心立方格子で8、面心立方格子で12、六方細密構造で12となります。
●体心立方格子の配位数
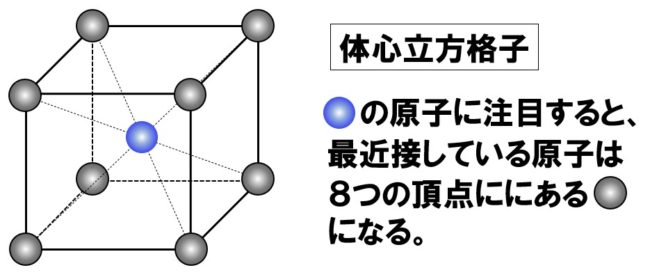
●面心立方格子の配位数
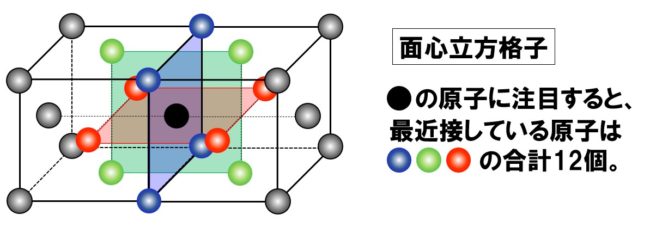
面心立方格子の配位数を考える場合、単位格子を上図のように2つ並べて、その中心にある原子に注目すると配位数が見えてきます。
●六方細密構造の配位数
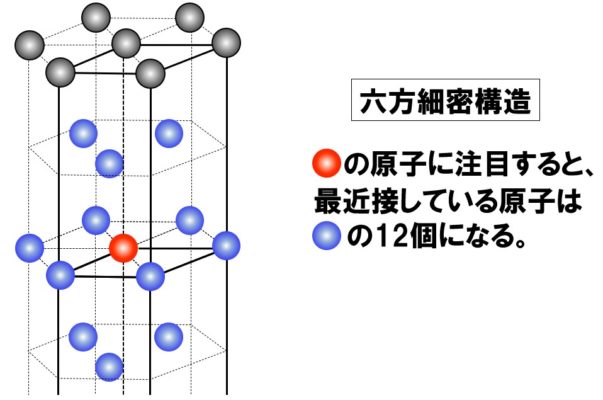
六方細密構造の配位数を考える際も、正六角柱を2つ重ね、その重ねた部分に位置する原子に注目すると配位数が見えてきます。
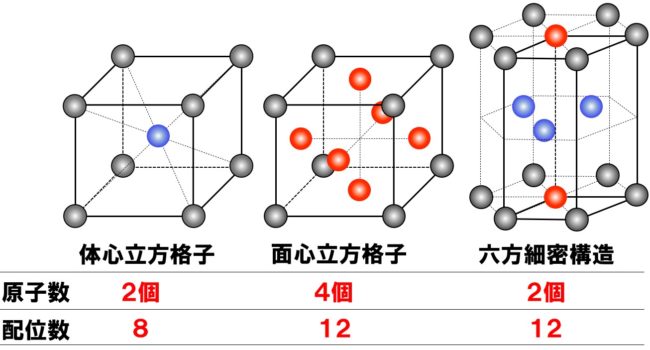
金属結晶の単位格子「原子数・配位数」まとめ
金属結晶の単位格子には、「体心立方格子」、「面心立方格子」、「六方細密構造」の3種類がありました。今回は単位格子内の原子数、配位数をしっかりとマスターしましょう。

コメント